천연 콜라겐 추출에 한외여과 적용
적용U한외여과E추출N자연적인C올라겐
Ⅰ.콜라겐이란?
콜라겐은 동물 결합 조직의 주요 구성 요소인 생체고분자이며 포유류에서 가장 풍부하고 널리 분포된 기능성 단백질로 전체 단백질의 25~30%를 차지하며 일부에서는 최대 80% 이상을 차지합니다. 유기체. 동물세포의 조직을 결합시키는 역할을 합니다.
측정에 따르면 성인의 체내에는 약 3kg의 콜라겐이 존재하며, 이는 주로 피부, 뼈, 눈, 치아, 힘줄, 내장기관(심장, 위, 장, 혈관 포함) 및 기타 부위에 존재합니다. 인체의. 그 기능은 피부와 장기의 형태와 구조를 유지하는 것이며, 손상된 조직을 복구하는 중요한 원료이기도 합니다.
II. 한외여과에 의한 잉어 비늘로부터 콜라겐 추출
1. 재료 및 방법
1.1 테스트 샘플
조 콜라겐의 수성 추출물.
1.2 테스트 방법
1.2.1 한외여과 공정
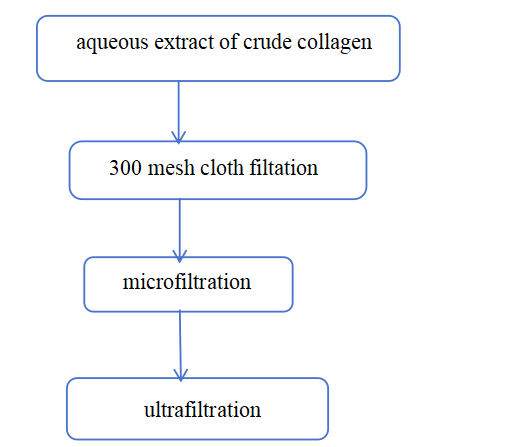
1.2.2 사전 여과 공정 결정
본 시험에서는 진공여과 방식과 정밀여과 방식의 비교 분석을 통해 최적의 전처리 여과 공정을 결정합니다. 구체적인 테스트 방법은 다음과 같습니다.
① 조콜라겐 수용성추출물을 여과지진공여과법으로 여과하여 수용성추출물 중의 부유입자 및 불순물을 제거한다.
② 조콜라겐 수용성추출물을 0.2μm 정밀여과막으로 여과하여 수용성추출물 중의 불용성물질, 불순물 등을 제거한다.
1.2.3 한외여과막 공극 크기 선택
정제 과정에서 한외여과막의 기공 크기는 100kDa입니다.
1.2.4 한외여과 정제 공정의 단일 인자 실험
조 콜라겐의 수성 추출물은 한외 여과 기술로 정제됩니다. 작동 압력, 작동 온도 및 pH가 콜라겐 유지에 미치는 영향에 대한 단일 요인 실험을 연구합니다. 일정 기간 동안 한외여과 장비를 시작한 후 다양한 요인이 콜라겐 유지율에 미치는 영향을 연구합니다.
1.2.5 계산식

2. 결과 및 분석
2.1 사전 여과 공정 분석
진공여과 방식과 정밀여과 방식의 비교 결과는 아래 표를 참조하세요.
|
여과 방법 |
여과 전 용액 농도/(g/L) |
여과 후 용액 농도/(g/L) |
감각 현상 |
|
진공 여과 방식 |
0.45 |
0.35 |
여과가 끝난 후에는 용액이 투명하지만 일정 시간 방치하면 용액이 탁해진다. |
|
미세여과 방식 |
0.45 |
0.42 |
여과가 끝난 후 용액은 투명해지고, 일정 시간 방치한 후에도 맑은 상태를 유지합니다. |
표에서 볼 수 있듯이 진공여과법과 정밀여과법 모두 용액 중의 불순물과 불용성 고형물을 제거할 수 있지만, 정밀여과법이 단백질에 대한 보호 효과가 더 우수하여 손실이 크지 않으며, 진공여과 방식은 단백질 손실이 발생할 수 있습니다. 또한, 진공여과에 의해 일정 시간 방치한 후 여액이 흐려지는 반면, 정밀여과는 여전히 맑고 투명하므로 한외여과의 전처리 공정으로 정밀여과를 선택한다.
2.2 한외여과 공정의 단일 요소 테스트
2.2.1 한외여과 압력이 보유율에 미치는 영향
온도 40도 및 pH 9.0의 조건에서 다양한 한외여과 압력(0.07MPa, 0.{)의 영향을 연구합니다. {11}}9MPa, 0.11MPa, 0.13MPa 및 0.15MPa) 단백질 보유율에 대한 값입니다. 결과는 아래 그림에 나와 있습니다.
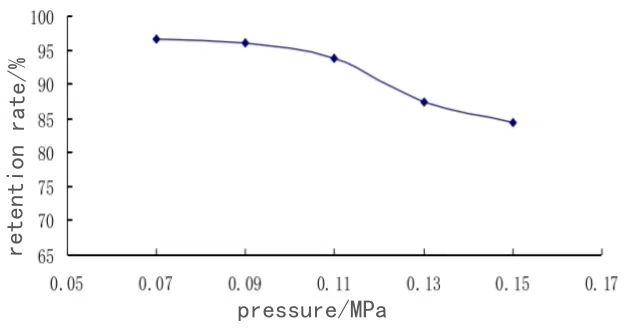
위 그림에서 알 수 있듯이, 운전압력이 증가함에 따라 단백질의 차단율은 점차 감소하였다. {{0}}.07MPa에서 단백질 유지율은 96.53%, 작동 압력이 0.15MPa일 때 단백질 유지율은 84.38%입니다. 한외여과에 의한 물질 분리는 압력차에 의해 이루어지기 때문입니다. 그 낮은 작동압력 범위에서는 저분자 물질은 빠르게 막을 통과할 수 있지만, 고분자 물질은 한외여과막에 갇혀 막 표면에 축적될 수 있으며, 이때 막 표면과 수용액 농도차 분극 저항을 유발하기 위해 농도차로부터 추출; 그러나 압력이 증가함에 따라 농도 분극 저항이 점차 증가하고 막 표면과 수성 추출물 사이의 농도 차이가 평형에 도달합니다. 압력이 이 평형을 초과하면 막 표면에 겔 층이 기록될 수 있습니다(이는 한외여과 중에 형성된 농도 분극 및 겔 층 이론과 일치함). 압력이 계속 증가하여 겔층의 두께가 증가하고, 막 표면에 남아있는 단백질이 증가하여 유지율이 낮아지게 됩니다. 멤브레인의 분리 효과를 보장하기 위한 최적의 작동 압력 매개변수는 0.07MPa입니다.
2.2.2 온도가 단백질 보유율에 미치는 영향
압력 {{0}}.11MPa, pH 9.0의 조건에서 다양한 온도(25도, 30도, 35도, 40도 및 45도)가 단백질 보유에 미치는 영향을 연구합니다. 결과는 아래 그림에 나와 있습니다.
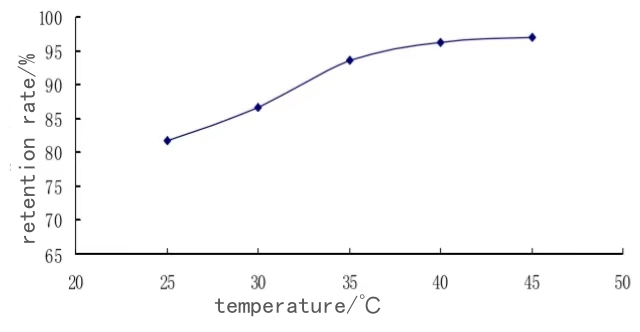
위 그림에서 보는 바와 같이, 온도가 증가함에 따라 한외여과막의 유지율은 점차 증가하여 45℃에서 최대치에 달하며, 유지율은 97.01%이다. 콜라겐의 점도는 온도와 밀접한 관련이 있기 때문에 온도가 낮을수록 콜라겐의 점도가 커지므로 콜라겐이 막 표면에 저항을 형성하기 쉽고 유지율이 낮습니다. 온도가 증가하면 콜라겐의 점도가 감소하고 콜라겐 분자간의 상호작용이 약화되어 물질전달율이 증가하고 농도분극이 약화되어 유지율이 증가하게 된다. 유지율이 증가하는 또 다른 이유는 온도가 증가함에 따라 콜라겐의 용해도가 증가하여 콜라겐이 막을 막는 현상이 감소하기 때문이다. 따라서 한외여과를 위한 최적온도는 45도이다.
2.2.3 단백질 보유에 대한 pH의 영향
압력 {{0}}.11MPa 및 온도 40도 조건에서 다양한 pH 조건, 즉 pH=6.0, pH{의 영향을 연구합니다. {5}}.{{1{12}}}}, pH=8.0, pH=9.0 및 pH=10.0, 유지율에 대한 . 결과는 아래 그림에 나와 있습니다.
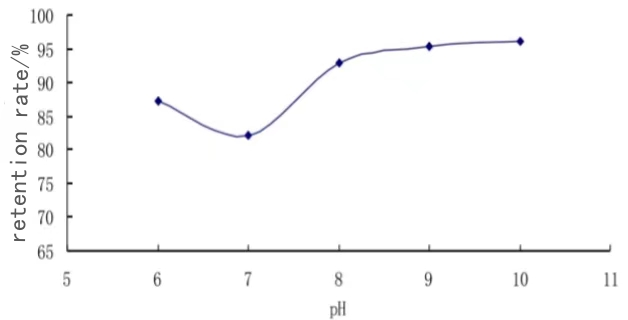
As shown in the above figure, within the pH value range of 6–7, with the increase of pH value, the protein retention rate decreases, and there is a minimum value of 82.13% at pH=7.0. When pH>7, with the increase of pH value, the retention rate gradually increases. This is because the isoelectric point of collagen pH=7, at the isoelectric point of protein is a precipitation state, easy to stay on the surface of the membrane block membrane, so that the retention rate is low; When pH>도 7에 나타낸 바와 같이, pH가 증가함에 따라 유지율은 점차 증가한다. 이는 한외여과막은 음전하를 띤 폴리에테르단풍막, 알칼리 조건에서 음전하를 띠는 콜라겐, 음전하를 띤 콜라겐 분자와 같은 전하를 띤 한외여과막이 상호 배타적인 상태를 형성하여 콜라겐 분자가 표면에 머물기 쉽지 않기 때문이다. 막의 경우 막을 차단하기가 쉽지 않으므로 한외여과의 최적 pH는 8-10입니다.
2.3 한외여과 공정 최적화 및 결과 검증
Design-Expert8.05 소프트웨어에 의한 분석에 따르면 최적의 공정 매개변수는 작동 압력 0.14MPa, 작동 온도 40.98도 및 용액 pH=9.43입니다. 이러한 조건에서 유지율은 92.551%였습니다. 실제 매개변수의 조작성을 고려하면 한외여과 조건에서 운전압력은 0.14MPa, 운전온도는 40도, 공급액의 pH값은 9.50이다. 실험적 검증은 한외여과 장치의 시스템이 안정되기 시작한 후에 시작됩니다. 얻은 유지율 결과는 (92.61 0.1)% (n=3)입니다. 방정식의 예측값은 기본적으로 측정값과 유사하며, 이는 예측된 조건부 매개변수 결과가 실제 조건부 결과와 일치함을 나타냅니다.
2.4 전기영동 분석 결과
정제된 콜라겐을 SDS-PAGE 전기영동으로 분석하고, 그 결과를 아래 그림에 나타내었다.

위 그림에서 볼 수 있듯이, 레인 1은 본 실험에서 정제된 콜라겐이고, 레인 2는 종아리 힘줄의 표준 콜라겐 샘플입니다. SDS-PAGE 전기영동을 통해 본 실험에서 제안한 콜라겐 단백질이 콜라겐임을 확인할 수 있었으나 겉보기에 불분명한 a1 펩타이드 사슬과 a2 펩타이드 사슬의 경계가 명확하지 않음을 알 수 있었다. 전기영동을 통해 다른 단백질 밴드가 없음을 알 수 있으며, 정제된 콜라겐의 순도가 높다는 결론을 내릴 수 있습니다.







